新着記事
癌細胞がワールブルク代謝移行時に活性化するPI3キナーゼ
メモリアルスローンケタリングキャンサーセンターは、癌細胞の動作について調査しています。研究は、ワールブルク代謝と、PI3キナーゼと呼ばれる細胞内の強力な酵素の活性との間の新しい関連性を発見しました。
Various hypotheses to explain the Warburg effect have been proposed over the years, including the idea that cancer cells have defective mitochondria — their “energy factories” — and therefore cannot perform the controlled burning of glucose. But none of these explanations has withstood the test of time. (Cancer cells’ mitochondria work just fine, for example.)
参照元:https://www.mskcc.org/news/sloan-kettering-institute-scientists-solve-100-year-old-mystery-about
– メモリアルスローンケタリングキャンサーセンター Memorial Sloan Kettering Cancer Center. January 21, 2021 –
概要:
- 1921年、ドイツの医師Otto Warburg氏は、癌細胞がブドウ糖からエネルギーを奇妙な非効率的な方法で収穫する事を観察
- 癌細胞は欠陥のあるミトコンドリアを持ち、その影響によりブドウ糖を燃焼しない
- それをワールブルク代謝と呼ぶ
- 免疫学者のMingLi氏の研究チームは、100年ぶりにワールブルク代謝と、PI3キナーゼの関連を発見
- PI3キナーゼは、細胞代謝の伝達機能を有するシグナル伝達分子
- 細胞分裂を含む、細胞内のエネルギーコストのかかる細胞イベントのほとんどは、PI3キナーゼが合図を出したときにのみ発生
- 細胞がワールブルク代謝に移行すると、PI3キナーゼの活性が高まり、細胞の分裂への取り組みが強化される
- 代謝を標的にすることが癌の成長を阻止する効果的な方法である可能性がある
科学者は癌についての100年前の謎を解きます
2021年は、すべての生化学の教科書で教えられている基本的な発見の100周年を迎えます。
1921年、ドイツの医師Otto Warburg氏は、癌細胞がブドウ糖からエネルギーを奇妙な非効率的な方法で収穫することを観察しました。
癌細胞は、酸素を使用して「燃焼」するのではなく、酵母が行うことを行います。
この酸素に依存しないプロセスはすぐに起こりますが、ブドウ糖のエネルギーの多くは未開発のままです。
癌細胞には欠陥のあるミトコンドリア(その「エネルギー工場」)があり、したがってブドウ糖の制御された燃焼を実行できないという考えを含め、ワールブルク効果を説明するさまざまな仮説が長年にわたって提案されてきました。
しかし、これらの説明はどれも時の試練に耐えることができませんでした。(たとえば、癌細胞のミトコンドリアは問題なく機能します。)
現在、免疫学者のMingLi氏が率いるSloanKettering Instituteの研究チームは、大量の遺伝的および生化学的実験に基づいて、1月21日にサイエンス誌に発表された答えを提供しています。
それは、ワールブルク代謝と、PI3キナーゼと呼ばれる細胞内の強力な酵素の活性との間のこれまで認識されていなかった関連性に帰着します。
Li博士は話します。
「PI3キナーゼは、細胞代謝の最高司令官のように機能する重要なシグナル伝達分子です。細胞分裂を含む、細胞内のエネルギーコストのかかる細胞イベントのほとんどは、PI3キナーゼが合図を出したときにのみ発生します。」
細胞がワールブルク代謝に移行すると、PI3キナーゼの活性が高まり、細胞の分裂への取り組みが強化されます。
これは、最高司令官にメガホンを渡すようなものです。
調査結果は、代謝を細胞シグナル伝達の二次的なものと見なす生化学者の間で一般的に受け入れられている見解を修正します。
彼らはまた、代謝を標的にすることが癌の成長を阻止する効果的な方法である可能性があることを示唆しています。
大学院生のKeXu氏を含むLi博士と彼のチームは、免疫細胞におけるワールブルク代謝を研究しました。
これも、この一見非効率的な代謝形態に依存しています。
免疫細胞が感染の存在を警告されると、T細胞と呼ばれる特定のタイプが、典型的な酸素燃焼型の代謝からワールブルク代謝に移行し、その数が増えて感染と戦う機構が強化されます。
このシフトを制御する重要なスイッチは、PI3キナーゼシグナル伝達に応答して作られる乳酸デヒドロゲナーゼA(LDHA)と呼ばれる酵素です。
この切り替えの結果、グルコースは部分的にしか分解されず、ATPと呼ばれる細胞のエネルギー通貨が細胞の細胞質ゾルで迅速に生成されます。
(対照的に、細胞が酸素を使用してブドウ糖を燃焼させると、部分的に分解された分子はミトコンドリアに移動し、そこでさらに分解されてATPを遅らせます。)
Li博士と彼のチームは、マウスでは、LDHAを欠くT細胞がPI3キナーゼ活性を維持できず、その結果、感染症と効果的に戦うことができないことを発見しました。
Li博士と彼のチームにとって、これはこの代謝酵素が細胞のシグナル伝達活性を制御していることを意味していました。
Li博士は話します。
「この分野は、代謝が成長因子シグナル伝達に続発するという仮定の下で機能してきました。言い換えれば、成長因子シグナル伝達は代謝を促進し、代謝は細胞の成長と増殖をサポートします。したがって、LDHAのような代謝酵素がPI3キナーゼを介した成長因子シグナル伝達に影響を与える可能性があるという観察は私たちの注目を集めました。」
他のキナーゼと同様に、PI3キナーゼはATPに依存して機能します。
ATPはワールブルク代謝の正味の産物であるため、ワールブルク代謝とPI3キナーゼ活性の間に正のフィードバックループが設定され、PI3キナーゼの継続的な活性、つまり細胞分裂が確保されます。
活性化された免疫細胞がこの形態の代謝に優先的に頼る理由については、Li博士は、細胞分裂と感染と戦う機構を強化するために、細胞がATPを迅速に生成する必要があることに関係していると考えています。
正のフィードバックループは、このプログラムが実行されると、感染が根絶されるまでそれが持続することを保証します。
チームは免疫細胞で発見をしましたが、癌との明確な類似点があります。
Li博士は話します。
「PI3キナーゼは、癌との関連で非常に重要なキナーゼです。これは、癌細胞が分裂するための成長シグナルを送るものであり、癌で最も活発なシグナル伝達経路の1つです。」
免疫細胞と同様に、癌細胞は、このシグナル伝達経路の活動を維持する方法としてワールブルク代謝を採用し、したがって、それらの継続的な成長と分裂を確実にする可能性があります。
この結果は、医師がLDHAの活動をブロックすることによって癌の増殖を抑制する可能性があるという興味深い可能性を高めています。
これはワールブルク代謝の「スイッチ」です。

この記事が気に入ったら
いいね または フォローしてね!
関連記事
新着記事
-

 男女ともに長生きになる「男女平等」2023.03.07健康
男女ともに長生きになる「男女平等」2023.03.07健康 -

 他者を犠牲にして利益を取る・利益を度外視して他者への害を取り除く2023.03.06人体・脳
他者を犠牲にして利益を取る・利益を度外視して他者への害を取り除く2023.03.06人体・脳 -

 「寿命を延ばす」良質な睡眠2023.03.05健康
「寿命を延ばす」良質な睡眠2023.03.05健康 -

 見極める力を養う「チャットボットの精度」2023.03.04技術
見極める力を養う「チャットボットの精度」2023.03.04技術 -

 健康増進と生きがいにつながる「森林浴」2023.03.03健康
健康増進と生きがいにつながる「森林浴」2023.03.03健康 -

 米国の6人に1人「肥満による死」2023.03.02健康
米国の6人に1人「肥満による死」2023.03.02健康 -

 週休4日制で生産を維持する2023.03.01社会
週休4日制で生産を維持する2023.03.01社会 -

 オンライン学習で学生に届く教育方法2023.02.28学習
オンライン学習で学生に届く教育方法2023.02.28学習 -

 学業成績に影響を与える「夜間の睡眠」2023.02.27健康
学業成績に影響を与える「夜間の睡眠」2023.02.27健康 -

 心の豊かさに大きく影響を与える「目的意識を持った10代の若者」2023.02.26健康
心の豊かさに大きく影響を与える「目的意識を持った10代の若者」2023.02.26健康
よく読まれている記事
-

 なぜタイピングより手書きの方が、記憶に定着するのか
なぜタイピングより手書きの方が、記憶に定着するのか -

 どんな曲が好き?「 音楽の好みと性格の関連性は普遍的 」
どんな曲が好き?「 音楽の好みと性格の関連性は普遍的 」 -

 視覚と意思決定領域の結びつきが強い「鮮明なイメージ能力がある人」
視覚と意思決定領域の結びつきが強い「鮮明なイメージ能力がある人」 -

 「触覚が敏感な部位はなぜあるのか」触覚メカニズムが解明される
「触覚が敏感な部位はなぜあるのか」触覚メカニズムが解明される -

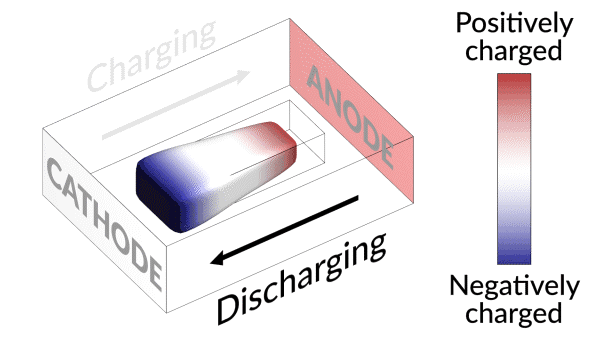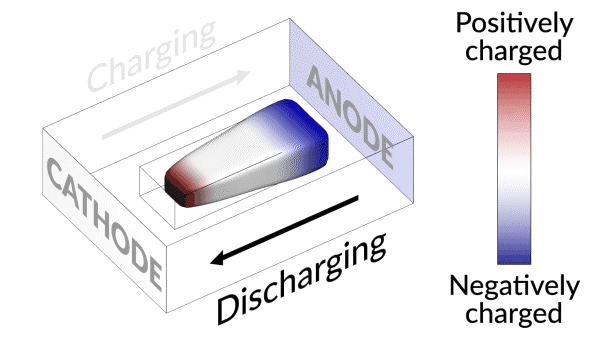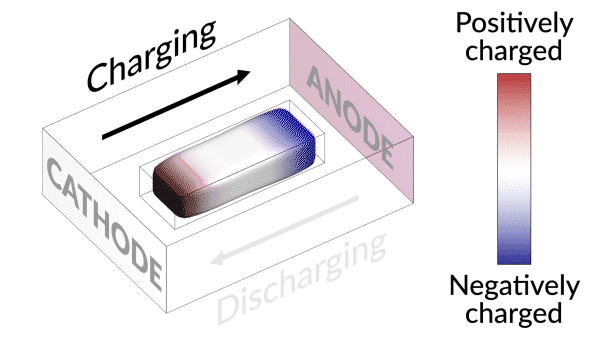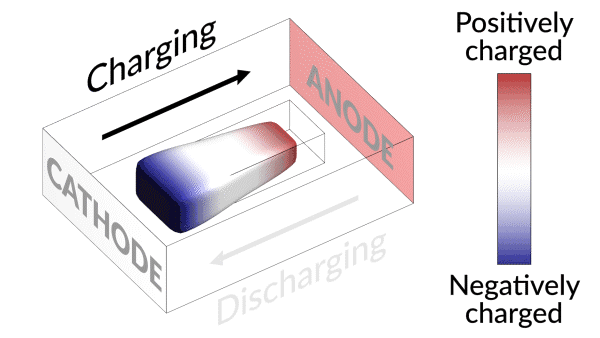 不活性化されたリチウムイオン電池を甦えさせる「復活するリチウムイオン電池」
不活性化されたリチウムイオン電池を甦えさせる「復活するリチウムイオン電池」 -

 記憶が脳に保存される新しい理論「MeshCODE理論」が開発される
記憶が脳に保存される新しい理論「MeshCODE理論」が開発される -

 大面積有機フォトダイオードに置き換わる?「シリコンフォトダイオード技術」
大面積有機フォトダイオードに置き換わる?「シリコンフォトダイオード技術」 -

 幸福度を7%上げる「旅行の仕方」
幸福度を7%上げる「旅行の仕方」 -

 「世界最長寿記録を更新し132歳まで生きる人が出現する」ベイズ統計学予測
「世界最長寿記録を更新し132歳まで生きる人が出現する」ベイズ統計学予測 -

 組織の中で行われたインシビリティ(非礼な言動)を軽視してはいけない理由
組織の中で行われたインシビリティ(非礼な言動)を軽視してはいけない理由
N E W S & P O P U L A R最 新 記 事 & 人 気 記 事
WHAT'S NEW !!
-






男女ともに長生きになる「男女平等」
【男女ともに長生きになる「男女平等」】 権利とは人間が作り出した構造ですが、男女平等が進むと男女ともに長生きになるようです。 The first global study to investi... -






他者を犠牲にして利益を取る・利益を度外視して他者への害を取り除く
【他者を犠牲にして利益を取る・利益を度外視して他者への害を取り除く】 他者を犠牲にして自分の利益を選ぶ、自分にとって利益は少ないが他者への害を防ぐ、道徳的なに... -






「寿命を延ばす」良質な睡眠
【「寿命を延ばす」良質な睡眠】 良質な睡眠をとることは、寿命を何年も長くする可能性があります。 Getting good sleep can play a role in supporting your heart and... -






見極める力を養う「チャットボットの精度」
【見極める力を養う「チャットボットの精度」】 ChatGPTをはじめ、チャットボットの精度は人が書いたものかどうかわからない程までの水準になっています。 The most rec...
-






なぜタイピングより手書きの方が、記憶に定着するのか
【なぜタイピングより手書きの方が、記憶に定着するのか】 ノルウェー科学技術大学の研究によると、手書きの方が物事をよく覚えることが判明しました。 様々なコンピュ... -






どんな曲が好き?「 音楽の好みと性格の関連性は普遍的 」
【どんな曲が好き?「 音楽の好みと性格の関連性は普遍的 」】 激しい音楽を好んで聴く人は、激しい性格の持ち主なのでしょうか?研究者は、音楽の好みと性格の関連性は... -






視覚と意思決定領域の結びつきが強い「鮮明なイメージ能力がある人」
【視覚と意思決定領域の結びつきが強い「鮮明なイメージ能力がある人」】 鮮明にイメージできる人は、視覚ネットワークと意思決定に関連する脳の領域が強く結びついてい...
News
- 新着記事 -
Popular
- 人気記事 -
H A P P I N E S S幸 福
人気 (❁´ω`❁)
M E A L食 事
B R A I N脳
人気 (❁´ω`❁)
H E A L T H健 康
人気 (❁´ω`❁)
-






人体・脳
健康な脳を保ち老化を遅らせる「アマゾンの先住民族ツィマネ族の生活習慣」
【健康な脳を保ち老化を遅らせる「アマゾンの先住民族ツィマネ族の生活習慣」】 ボリビア・アマゾンの先住民族であるツィマネ族が、アメリカやヨーロッパの人々に比べて... -






社会
自制心が健康と若さをもたらす理由
【自制心が健康と若さをもたらす理由】 デューク大学の研究チームは、自制心が心身に及ぼす影響を調査しました。 1000人を出生から45年間に渡って追跡した大規模調査で... -






健康
高強度インターバルトレーニングは、適度な運動よりも心臓を強化する
【心臓を強化する高強度インターバルトレーニング】 ノルウェー科学技術大学の研究によると、トレーニングの強度が、病気の重症度を軽減し、心臓機能を改善し、作業能力...
-






人体・脳
健康な脳を保ち老化を遅らせる「アマゾンの先住民族ツィマネ族の生活習慣」
【健康な脳を保ち老化を遅らせる「アマゾンの先住民族ツィマネ族の生活習慣」】 ボリビア・アマゾンの先住民族であるツィマネ族が、アメリカやヨーロッパの人々に比べて... -






社会
自制心が健康と若さをもたらす理由
【自制心が健康と若さをもたらす理由】 デューク大学の研究チームは、自制心が心身に及ぼす影響を調査しました。 1000人を出生から45年間に渡って追跡した大規模調査で... -






健康
高強度インターバルトレーニングは、適度な運動よりも心臓を強化する
【心臓を強化する高強度インターバルトレーニング】 ノルウェー科学技術大学の研究によると、トレーニングの強度が、病気の重症度を軽減し、心臓機能を改善し、作業能力...
J O B仕 事
人気 (❁´ω`❁)
-






社会
週休4日制で生産を維持する
-






人体・脳
アイデアや閃きが降りてくる「横断的なコミュニケーション」
-





社会
大災害を読み解く鋭い解決策
-






思考・瞑想
賞や表彰が発明家の創造性を低下させる
-






人体・脳
創造的な人はここが違う!「非創造的なハブを回避し非典型的なアプローチをする」
-






社会
アメリカ陸軍で既に多数の成功を収めている「人々を創造的にするトレーニング」
-






社会
2年は普及しない?「カテゴリーイノベーション戦略」
-






社会
管理者級以上必見「創造性を引き出す同僚間の友情とサポートを育む組織づくり」
-






社会
アイデアを創出する人数「少人数のグループのほうが新しいアイデアが出やすい」
-






健康
散った気を元の集中に戻す「1日最大50%費やす迷いを断つマインドフルネス」
-





社会
移動によるエネルギーが激減「環境に優しく誰でも参加できるオンライン会議」
-






社会
山火事コスト数十億ドルのコスト削減「インドネシアの泥炭地回復」
-






社会
価格末「99円」設定が販売者に不利益を及ぼす驚愕の理由
-






社会
購買意欲を掻き立てる商品提示方法
-






社会
「感情的異質性」がチームの創造性を高める
-






社会
従業員の創造性を高める驚愕の方法「報酬を選択制にする」
-






社会
テクノロジーの力でセレンディピティを生み出す
-






社会
様々なテーマの問題への取り組みにつながる「ダ・ヴィンチ構想」
-






社会
改善が必要な状況に「やめる」という解決策がでない理由
-






社会
空想が苦手な理由と、その修正方法
-






学習
パズル解きの極意、最良の選択より優れた驚愕の方法
-






社会
大麻が独創的で実現不可能なアイデアを創出するという実験結果
-






社会
記憶に残るユーモアを含んだニュース
-





社会
なぜメッセージと画像が一致してない情報は伝わらないのか
-






社会
消費者を購買に結びつける音楽
-






技術
自動化工場などの緊急事態に備えて知識を生かしておく方法
-






社会
「生産性も顧客満足度も向上」プロジェクトに自主性を持たせる
-






人体・脳
人は1日に35,000回の意思決定をしている「意思決定を行うアルゴリズム」
-






社会
他文化と頻繁衝突する文化圏は協力的なゲームが流行?「ゲームからみる文化」
-






社会
「通勤はわるいもの?」モバイルセンシングで仕事の成果と通勤の関連性を解明
-






社会
テクノロジーは労働者の幸福度にどのような影響を及ぼすか
-






社会
雇用の創出ではなく雇用の置換が進む「ロボットなどの作業の自動化」
-






社会
「柔軟で弾力性のある対応が可能」生物系を模倣した多様なサプライチェーン
-






社会
「患者のメンタルヘルスケアを向上させる」患者と心理療法士のマッチング
-




学習
デジタルデバイス用に最適なフォント「AdaptiFont」
T E C H N O L O G Y技 術
人気 (❁´ω`❁)