新着記事
グラフィカルモデルを使用して「病気に罹患するメカニズム」を特定
ジョージア工科大学の研究チームは、グラフィカルモデルなどの既存のツールを用いて細胞を識別し、病気のメカニズムを理解する方法を発見しました。
病気の理解・診断・治療に大きく貢献する事が期待されます。
A multidisciplinary team of Georgia Institute of Technology neuroscience researchers, borrowing from existing tools such as graphical models, have uncovered a better way to identify cells and understand the mechanisms of the diseases, potentially leading to better understanding, diagnosis, and treatment.
参照元:https://news.gatech.edu/2021/03/17/identifying-cells-better-understand-healthy-and-diseased-behavior
– ジョージア工科大学 Georgia Institute of Technology. MARCH 17, 2021 –
アルツハイマー病やパーキンソン病などの変性状態の原因と潜在的な治療法を研究する際、神経科学者は、記憶力の低下や平衡障害や震えなどの行動変化を引き起こす脳活動を理解するために必要な細胞を正確に特定するのに苦労することがよくあります。
ジョージア工科大学の神経科学研究者の学際的なチームは、グラフィカルモデルなどの既存のツールを借りて、細胞を識別し、病気のメカニズムを理解するためのより良い方法を発見しました。
これは、より良い理解、診断、および治療につながる可能性があります。
彼らの調査結果は、2021年2月24日にジャーナルeLifeで報告されました。
この研究は、国立衛生研究所と国立科学財団によってサポートされていました。
神経科学の分野では、神経系がどのように機能し、遺伝子と環境が行動にどのように影響するかを研究しています。
神経科学者は、新しいテクノロジーを使用して生物学的システムの自然な状態と機能不全の状態を理解することにより、最終的に病気を治療することを望んでいます。
それが起こる前に、神経科学者はまず脳内のどの細胞が行動を促進しているのかを理解する必要がありますが、細胞ごとの脳活動のマッピングは見た目ほど簡単ではありません。
2つの脳細胞は同じではありません
ジョージア工科大学の化学および生体分子工学の学校で、化学および生体分子工学のラブファミリー教授であるHangLu氏は話します。
「伝統的に、科学者は画像をアトラスと比較することによって各細胞の位置をマッピングする座標系を確立しましたが、「すべての脳が同じように見える」という文献の概念は絶対に真実ではありません。」
協調的アプローチを取ることは、2つの主要な課題を提示します。
1つは、セルの数が非常に多く、どれもそれほど明確に見えないことです。
第二に、細胞は個人によって異なります。
Lu氏は話します。
「これは現在の大きなボトルネックです。ニューロンの活動を好きなだけ記録できますが、どの細胞が何をしているのかがわからない場合、脳や状態を比較して意味のある結論を出すことは困難です。」
大学院の研究者ShiveshChaudharyによると、データにはノイズがあり、脳の2つの異なる領域間の対応を確立するのが困難です。
Lu氏は話します。
「データにいくつかの変形が存在するか、形状の一部が欠落している可能性があります。」
地理だけでなく、細胞の関係に焦点を当てる
これらの課題を克服するために、Georgia Techの研究者は、機械学習のグラフィカルモデルと数学の形状マッチングへのメトリックジオメトリアプローチの2つの分野から借用し、モデル生物である線虫C.elegansの細胞を特定する計算方法を構築しました。
チームは、自然言語処理などの他の分野のフレームワークを使用して、独自のモデリングソフトウェアを構築しました。
自然言語処理では、コンピューターはステートメント内の単語間の依存関係をキャプチャすることにより、文の意味を判別できます。
研究者たちは同様のモデルを採用しましたが、「細胞を識別するためにニューロン間でそれらをキャプチャしました」という単語間の依存関係をキャプチャする代わりに、このアプローチは各セルの地理的位置を調べる他の方法と比較してエラー伝播を制限することに注意しました。
Lu氏は話します。
「セル間の関係を使用することは、実際にはセルのアイデンティティを定義する上でより有用でした。1つを定義すると、他のセルのアイデンティティに影響を与えることになります。」
研究チームによると、このアプローチは現在の識別方法よりもはるかに正確です。
アルゴリズムは完全ではありませんが、不完全なデータに直面しても大幅にパフォーマンスが向上し、ノイズやエラーによる「ガタガタ音が少なくなる」とLu氏は述べています。
科学者が病気のメカニズムを理解すると、介入を見つけることができるため、このアルゴリズムは多くの発達疾患に大きな影響を及ぼします。
Lu氏は話します。
「これを使用して、遺伝的リスクを評価するための薬物および遺伝的スクリーニングを行うことができます。誰かの遺伝的背景を取得し、この背景によって細胞が標準の参照遺伝的背景とどのように異なるかを調べることができます。」
ハーバード大学脳科学センターの生物進化生物学部教授であるユン・チャン氏は話します。
「このアプローチの優れた点の1つは、データ駆動型であるため、個々のワーム間の変動をキャプチャすることです。この方法は、正常な状態だけでなく、病気の下での発達と機能に関する幅広い研究に適用できる可能性が高いです。」
より高速なデータ分析
このアルゴリズムは、脳全体のデータを分析する速度を大幅に加速します。
研究者たちは、この進歩の前に、彼らの研究室が一連のデータを記録するのに20分かかるかもしれませんが、細胞を特定してデータを分析するのに数週間かかるだろうと説明しました。
アルゴリズムを使用すると、分析は「デスクトップ上でせいぜい一晩」かかります、とChaudhary氏は言いました。
この手法は、アルゴリズムをテストしてアトラスを構築できる、より大きなコミュニティにアルゴリズムを開放するクラウドソーシングのコラボレーションオンラインプラットフォームもサポートします。
Lu氏は話します。
「同じ問題に取り組んでいるすべての研究者は、記録を行い、すべての状況で広く使用できるこれらのアトラスのさらなる構築に貢献することができます。」
研究者たちは、物理学、生物学、数学、化学にまたがる複数の分野を利用できることで、プロジェクトの成功を認めています。
化学工学の学士号を持っているChaudhary氏は、この特定の神経科学の問題を解決するために、コンピューターサイエンスと数学の発展を利用しました。
Chaudhary氏は続けます。
「私たちの研究室には、顕微鏡の構築に取り組んでいる物理学者、生物学者、コンピューターサイエンスに傾倒している私のような人々がいます。純粋数学者とも協力しています。神経科学の分野にはすべてがあります。あなたはあなたが望むどんな方向にも行くことができます。」


この記事が気に入ったら
いいね または フォローしてね!
関連記事
新着記事
-

 男女ともに長生きになる「男女平等」2023.03.07健康
男女ともに長生きになる「男女平等」2023.03.07健康 -

 他者を犠牲にして利益を取る・利益を度外視して他者への害を取り除く2023.03.06人体・脳
他者を犠牲にして利益を取る・利益を度外視して他者への害を取り除く2023.03.06人体・脳 -

 「寿命を延ばす」良質な睡眠2023.03.05健康
「寿命を延ばす」良質な睡眠2023.03.05健康 -

 見極める力を養う「チャットボットの精度」2023.03.04技術
見極める力を養う「チャットボットの精度」2023.03.04技術 -

 健康増進と生きがいにつながる「森林浴」2023.03.03健康
健康増進と生きがいにつながる「森林浴」2023.03.03健康 -

 米国の6人に1人「肥満による死」2023.03.02健康
米国の6人に1人「肥満による死」2023.03.02健康 -

 週休4日制で生産を維持する2023.03.01社会
週休4日制で生産を維持する2023.03.01社会 -

 オンライン学習で学生に届く教育方法2023.02.28学習
オンライン学習で学生に届く教育方法2023.02.28学習 -

 学業成績に影響を与える「夜間の睡眠」2023.02.27健康
学業成績に影響を与える「夜間の睡眠」2023.02.27健康 -

 心の豊かさに大きく影響を与える「目的意識を持った10代の若者」2023.02.26健康
心の豊かさに大きく影響を与える「目的意識を持った10代の若者」2023.02.26健康
よく読まれている記事
-

 なぜタイピングより手書きの方が、記憶に定着するのか
なぜタイピングより手書きの方が、記憶に定着するのか -

 どんな曲が好き?「 音楽の好みと性格の関連性は普遍的 」
どんな曲が好き?「 音楽の好みと性格の関連性は普遍的 」 -

 視覚と意思決定領域の結びつきが強い「鮮明なイメージ能力がある人」
視覚と意思決定領域の結びつきが強い「鮮明なイメージ能力がある人」 -

 「触覚が敏感な部位はなぜあるのか」触覚メカニズムが解明される
「触覚が敏感な部位はなぜあるのか」触覚メカニズムが解明される -

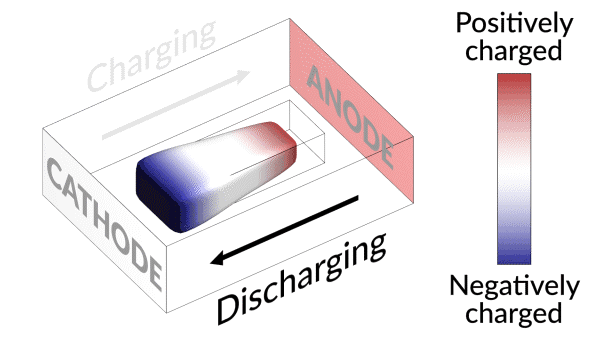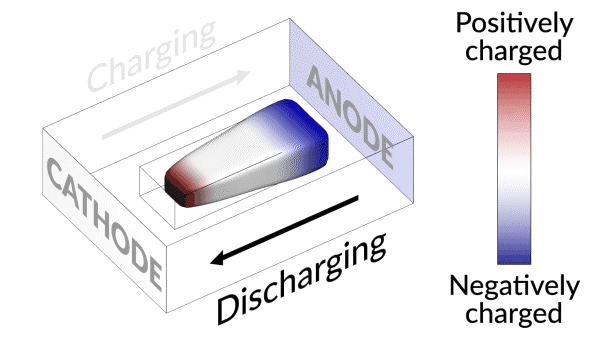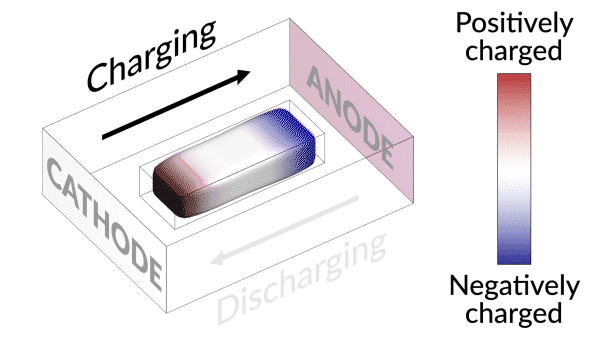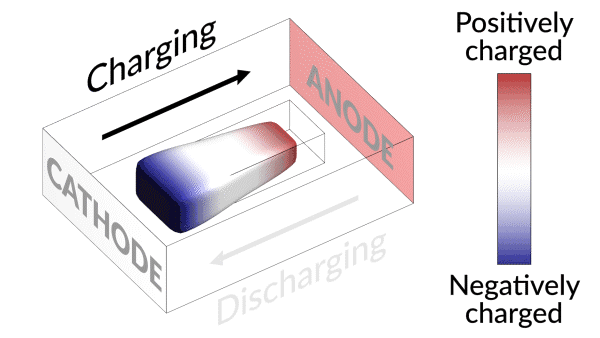 不活性化されたリチウムイオン電池を甦えさせる「復活するリチウムイオン電池」
不活性化されたリチウムイオン電池を甦えさせる「復活するリチウムイオン電池」 -

 記憶が脳に保存される新しい理論「MeshCODE理論」が開発される
記憶が脳に保存される新しい理論「MeshCODE理論」が開発される -

 大面積有機フォトダイオードに置き換わる?「シリコンフォトダイオード技術」
大面積有機フォトダイオードに置き換わる?「シリコンフォトダイオード技術」 -

 幸福度を7%上げる「旅行の仕方」
幸福度を7%上げる「旅行の仕方」 -

 「世界最長寿記録を更新し132歳まで生きる人が出現する」ベイズ統計学予測
「世界最長寿記録を更新し132歳まで生きる人が出現する」ベイズ統計学予測 -

 組織の中で行われたインシビリティ(非礼な言動)を軽視してはいけない理由
組織の中で行われたインシビリティ(非礼な言動)を軽視してはいけない理由
N E W S & P O P U L A R最 新 記 事 & 人 気 記 事
WHAT'S NEW !!
-






男女ともに長生きになる「男女平等」
【男女ともに長生きになる「男女平等」】 権利とは人間が作り出した構造ですが、男女平等が進むと男女ともに長生きになるようです。 The first global study to investi... -






他者を犠牲にして利益を取る・利益を度外視して他者への害を取り除く
【他者を犠牲にして利益を取る・利益を度外視して他者への害を取り除く】 他者を犠牲にして自分の利益を選ぶ、自分にとって利益は少ないが他者への害を防ぐ、道徳的なに... -






「寿命を延ばす」良質な睡眠
【「寿命を延ばす」良質な睡眠】 良質な睡眠をとることは、寿命を何年も長くする可能性があります。 Getting good sleep can play a role in supporting your heart and... -






見極める力を養う「チャットボットの精度」
【見極める力を養う「チャットボットの精度」】 ChatGPTをはじめ、チャットボットの精度は人が書いたものかどうかわからない程までの水準になっています。 The most rec...
-






なぜタイピングより手書きの方が、記憶に定着するのか
【なぜタイピングより手書きの方が、記憶に定着するのか】 ノルウェー科学技術大学の研究によると、手書きの方が物事をよく覚えることが判明しました。 様々なコンピュ... -






どんな曲が好き?「 音楽の好みと性格の関連性は普遍的 」
【どんな曲が好き?「 音楽の好みと性格の関連性は普遍的 」】 激しい音楽を好んで聴く人は、激しい性格の持ち主なのでしょうか?研究者は、音楽の好みと性格の関連性は... -






視覚と意思決定領域の結びつきが強い「鮮明なイメージ能力がある人」
【視覚と意思決定領域の結びつきが強い「鮮明なイメージ能力がある人」】 鮮明にイメージできる人は、視覚ネットワークと意思決定に関連する脳の領域が強く結びついてい...
News
- 新着記事 -
Popular
- 人気記事 -
H A P P I N E S S幸 福
人気 (❁´ω`❁)
M E A L食 事
B R A I N脳
人気 (❁´ω`❁)
H E A L T H健 康
人気 (❁´ω`❁)
-






人体・脳
健康な脳を保ち老化を遅らせる「アマゾンの先住民族ツィマネ族の生活習慣」
【健康な脳を保ち老化を遅らせる「アマゾンの先住民族ツィマネ族の生活習慣」】 ボリビア・アマゾンの先住民族であるツィマネ族が、アメリカやヨーロッパの人々に比べて... -






社会
自制心が健康と若さをもたらす理由
【自制心が健康と若さをもたらす理由】 デューク大学の研究チームは、自制心が心身に及ぼす影響を調査しました。 1000人を出生から45年間に渡って追跡した大規模調査で... -






健康
高強度インターバルトレーニングは、適度な運動よりも心臓を強化する
【心臓を強化する高強度インターバルトレーニング】 ノルウェー科学技術大学の研究によると、トレーニングの強度が、病気の重症度を軽減し、心臓機能を改善し、作業能力...
-






人体・脳
健康な脳を保ち老化を遅らせる「アマゾンの先住民族ツィマネ族の生活習慣」
【健康な脳を保ち老化を遅らせる「アマゾンの先住民族ツィマネ族の生活習慣」】 ボリビア・アマゾンの先住民族であるツィマネ族が、アメリカやヨーロッパの人々に比べて... -






社会
自制心が健康と若さをもたらす理由
【自制心が健康と若さをもたらす理由】 デューク大学の研究チームは、自制心が心身に及ぼす影響を調査しました。 1000人を出生から45年間に渡って追跡した大規模調査で... -






健康
高強度インターバルトレーニングは、適度な運動よりも心臓を強化する
【心臓を強化する高強度インターバルトレーニング】 ノルウェー科学技術大学の研究によると、トレーニングの強度が、病気の重症度を軽減し、心臓機能を改善し、作業能力...
J O B仕 事
人気 (❁´ω`❁)
-






社会
週休4日制で生産を維持する
-






人体・脳
アイデアや閃きが降りてくる「横断的なコミュニケーション」
-





社会
大災害を読み解く鋭い解決策
-






思考・瞑想
賞や表彰が発明家の創造性を低下させる
-






人体・脳
創造的な人はここが違う!「非創造的なハブを回避し非典型的なアプローチをする」
-






社会
アメリカ陸軍で既に多数の成功を収めている「人々を創造的にするトレーニング」
-






社会
2年は普及しない?「カテゴリーイノベーション戦略」
-






社会
管理者級以上必見「創造性を引き出す同僚間の友情とサポートを育む組織づくり」
-






社会
アイデアを創出する人数「少人数のグループのほうが新しいアイデアが出やすい」
-






健康
散った気を元の集中に戻す「1日最大50%費やす迷いを断つマインドフルネス」
-





社会
移動によるエネルギーが激減「環境に優しく誰でも参加できるオンライン会議」
-






社会
山火事コスト数十億ドルのコスト削減「インドネシアの泥炭地回復」
-






社会
価格末「99円」設定が販売者に不利益を及ぼす驚愕の理由
-






社会
購買意欲を掻き立てる商品提示方法
-






社会
「感情的異質性」がチームの創造性を高める
-






社会
従業員の創造性を高める驚愕の方法「報酬を選択制にする」
-






社会
テクノロジーの力でセレンディピティを生み出す
-






社会
様々なテーマの問題への取り組みにつながる「ダ・ヴィンチ構想」
-






社会
改善が必要な状況に「やめる」という解決策がでない理由
-






社会
空想が苦手な理由と、その修正方法
-






学習
パズル解きの極意、最良の選択より優れた驚愕の方法
-






社会
大麻が独創的で実現不可能なアイデアを創出するという実験結果
-






社会
記憶に残るユーモアを含んだニュース
-





社会
なぜメッセージと画像が一致してない情報は伝わらないのか
-






社会
消費者を購買に結びつける音楽
-






技術
自動化工場などの緊急事態に備えて知識を生かしておく方法
-






社会
「生産性も顧客満足度も向上」プロジェクトに自主性を持たせる
-






人体・脳
人は1日に35,000回の意思決定をしている「意思決定を行うアルゴリズム」
-






社会
他文化と頻繁衝突する文化圏は協力的なゲームが流行?「ゲームからみる文化」
-






社会
「通勤はわるいもの?」モバイルセンシングで仕事の成果と通勤の関連性を解明
-






社会
テクノロジーは労働者の幸福度にどのような影響を及ぼすか
-






社会
雇用の創出ではなく雇用の置換が進む「ロボットなどの作業の自動化」
-






社会
「柔軟で弾力性のある対応が可能」生物系を模倣した多様なサプライチェーン
-






社会
「患者のメンタルヘルスケアを向上させる」患者と心理療法士のマッチング
-




学習
デジタルデバイス用に最適なフォント「AdaptiFont」
T E C H N O L O G Y技 術
人気 (❁´ω`❁)